(Actualizada 11-abr-2021)
Nota: dos presentaciones basadas en los artículos de esta serie sobre la ciencia del buceo están disponibles aquí (52:30) y aquí (1:12:00).
Introducción
Esta es la tercera entrada de una serie sobre la ciencia del buceo: los efectos que produce en nuestro cuerpo y cómo los mitigamos.
En la primera entrada tratamos la situación de inmersión, cómo resolvemos el respirar bajo el agua así como la pérdida de calor. La segunda versó sobre las dificultades para el desplazamiento, los efectos de flotabilidad y cómo la inmersión afecta a la percepción por parte de nuestros sentidos. En esta tercera y última, discutimos los grandes cambios de presión que experimenta el organismo en el medio acuático y las consecuencias que provoca.
Presión de inmersión
El 11 de junio de 1644, el físico y matemático Evangelista Torricelli escribió una carta a su amigo y también matemático el cardenal Michelangelo Ricci, en la que podía leerse:
Vivimos sumergidos en el fondo de un océano del elemento aire, el cual, por incuestionables experiencias, se sabe que tiene peso.
– Evangelista Torricelli
Su maestro Galileo Galilei había iniciado el estudio de la fuerza que ejerce el aire sin llegar a resolver el problema, mediado como se encontraba por la idea aristotélica del horror vacui que propugnaba que la naturaleza aborrecía el vacío, con lo que un espacio que no contuviese aire era imposible. Pero en 1643, Torricelli abordó el problema experimentando con distintos tubos de mercurio hasta determinar que la presión viene dada por la columna de aire de la atmósfera sobre nuestras cabezas, que equivale a una de mercurio de 760 mm de altura.

Los 760 mm de mercurio de Torricelli corresponden a la presión atmosférica a nivel del mar, lo que define la unidad de presión llamada atmósfera estandard (atm). Cuando ascendemos, la columna de aire encima de nosotros disminuye, y con ella la presión, pero no de forma lineal con la altura porque el aire es compresible, lo que da lugar a la fórmula barométrica: hay que subir hasta 2000 m de altura para que la presión atmosférica se reduzca hasta las 0.8 atmósferas. Esta es una presión habitual en las cabinas de los aviones, y por eso las bolsas de patatas, semillenas en la fábrica con aire a una atmósfera de presión, tienen ese aspecto hercúleo durante el vuelo: el aire del interior de la bolsa está a mayor presión que el entorno y se expande.
Fun little science tidbit on my recent flight: a bag of chips expands as the plane ascends. Why? Because as altitude increases, pressure decreases. There are less air particles pressing on the outside of the bag, therefore the air on the inside of the bag will expand outward 🤓 pic.twitter.com/cRcPclwpP0
— Kelsey Lucerne (@KelseyLucerne) June 3, 2019
Si subimos un puerto muy alto con la bolsa de patatas en el salpicadero del coche, llega un momento en que la bolsa no es capaz de aguantar la diferencia entre la presión interna y la externa y estalla (en el video que sigue, Pressure se refiere a esa diferencia de presión).
¿Pero que pasa con un fluido incompresible como el agua? En este caso la presión viene dada por la ecuación fundamental de la hidrostática donde
es la densidad del fluido,
la aceleración de la gravedad y
la altura de la columna [Ecuación hidrostática]. Como la densidad del agua es unas 830 veces la del aire, resulta que basta una columna de 10 m de agua para producir la misma presión que toda la atmósfera. En otras palabras: a diez metros de profundidad la presión ejercida por el agua es una atmósfera.
Pero esa no es la única presión que actúa sobre el cuerpo del buceador. El principio de Pascal establece que toda presión ejercida sobre un fluido se transmite en su seno en todas las direcciones, con lo que la presión total a cierta profundidad viene dada por la suma de las presiones hidrostática (
, del agua) más la atmosférica (
, del aire):
.
Que la presión sea la misma en todos los puntos de un líquido situados a la misma profundidad, independientemente de la forma del recipiente que lo contiene, explica la denominada paradoja hidrostática o paradoja de Pascal, ilustrada con el experimento del rompetoneles de Pascal: un tonel de madera lleno de agua, coronado por un tubo largo por el que se vierte agua estalla cualquiera que sea la sección del tubo [Tonel Pascal].

Por tanto, la presión total a 10 m de profundidad es la suma de las presiones producidas por la atmósfera y por la columna de agua, cada una de las cuales es una atmósfera y suman dos, que a veces se expresa como “2 ATA” que significa “atmósferas absolutas” [Diccionario buceo]. Más aún, por cada 10 m extra de profundidad, otra atmósfera que tenemos que soportar, con lo que a 30 m, la profundad máxima recomendada para el buceo recreativo, la presión de inmersión (ver la ilustración 8 de la primera entrada de esta serie) es de unas cuatro atmósferas (4 ATA).

En el siguiente video el astronauta Chris Hadfield está entrenándose en un hábitat submarino (ver la sección «buceo de saturación» de la primera entrada de esta serie) a 15 metros de profundidad, y por tanto a unas 2.5 ATA. Ha cogido una lata de bebida gaseosa y la ha agitado vigorosamente, pero al abrirla no salpica ni se derrama porque la presión del CO disuelto en el interior de la lata es de unas 1.6 atmósferas, inferior a la del entorno.
This is what happens when you shake a can of soda and open it on the ocean floor 😲😲 pic.twitter.com/9DU3s4qUJY
— UNILAD Tech (@UNILADTECH) November 6, 2019
Efectos de la presión sobre el buceador
Vemos entonces que buceando la presión puede ser bastante alta pero… ¿qué efectos tienen esas presiones sobre el buceador? Se pueden distinguir dos tipos : por una parte los debidos a la presión total sobre nuestro cuerpo y por otra las consecuencias de la presión de cada gas individual presente en la mezcla que respiramos.
Para una discusión compacta de cómo los mamíferos marinos lidian con los efectos de la presión recomiendo las tres entradas (esta, esta y esta) de Juan Ignacio Perez en su blog Zoo Logik.
Efectos de la presión neta
En realidad a la mayor parte de nuestro cuerpo el aumento de presión le da un poco igual porque estamos hechos de agua y tejidos netamente incompresibles. Pero tenemos algunos espacios aéreos, tanto naturales (como los pulmones, boca, senos nasales y trompa de Eustaquio) como artificiales (el creado en nuestra cara por la máscara de buceo). ¿Y qué ocurre con los gases bajo presión? Nos lo contaron Boyle y Mariotte con su ley: a temperatura constante, el producto de la presión por el volumen de un gas es constante; esto es, al aumentar la presión disminuye el volumen y aumenta la densidad del gas.


Al descender en una inmersión nuestros oídos pueden llegar a doler ligeramente por la diferencia de presión a ambos lados del tímpano. Para evitarlo hay que descender despacio y compensar esa diferencia de presión, si es necesario incluso forzando el aire de la garganta hacia los senos y el tímpano, maniobra que se conoce como de Valsalva por el médico italiano Antonio Maria Valsalva [Valsalva], que tiene utilidad en diagnóstico de hernias inguinales y/o lumbares, tratamiento de algunos soplos y taquicardias, y se usa también en halterofilia y entrenamiento de fuerza, si bien no está exenta de cierta polémica como nos explicó Francisco Canales en la entrada de Naukas No te salva entrenar con Valsalva. Algunos trajes espaciales y cascos profesionales de buceo incorporan un «dispositivo Valsalva» que permite a los astronautas o buceadores hacer la maniobra de Valsalva sin tener que usar sus manos para bloquear la nariz.

Pero, ¿qué ocurrirá con nuestros pulmones si mantenemos cerrada la vía aérea al ascender tras una inmersión?

Pues ocurrirá que el aire de los pulmones va a triplicar su volumen (suponiendo que estuviésemos a 20 m) con lo que los setecientos millones de globitos que contienen y que llamamos alveolos no lo van a llevar bien. Es lo que se denomina barotrauma, un daño físico en los tejidos situados entre el espacio aéreo interno y el fluido que lo rodea y que puede ir desde meras hemorragias en los senos faciales, pasando por rotura del tímpano, hasta embolia o neumotórax. Hay incluso casos documentados de burbujas de aire que se alojan en una caries y que cuando asciende el buceador ¡hacen estallar la muela! [Ranna 2016].
Afortunadamente la forma de evitar el barotrauma buceando es bien sencilla: ¡respirar!
La regla más importante del buceo con equipo autónomo es respirar continuamente: nunca, nunca aguantar la respiración. El equipo de buceo aporta aire a una presión igual a la del agua circundante, con lo cual los pulmones estarán siempre en equilibrio, conservarán su volumen normal a cualquier profundidad y la posibilidad de barotrauma desaparece.
Efectos de cada gas individual
El aire de la atmósfera está compuesto por un 78% de nitrógeno, un 21% de oxígeno, casi un 1% de argón y pequeñas cantidades de otros gases, fundamentalmente dióxido de carbono, que combinados suman aproximadamente un 0.1%. Eso el aire seco, porque el vapor de agua varía su proporción entre un 0 y un 4% dependiendo del lugar donde te encuentres, la hora del día y el tiempo meteorológico.
¿Cuáles son las presiones parciales de los dos gases mayoritarios? Para ello hemos de echar mano de la ley de Dalton enunciada en 1802 por John Dalton: la presión de una mezcla de gases, que no reaccionan químicamente, es igual a la suma de las presiones parciales que ejercería cada uno de ellos si ocupase todo el volumen de la mezcla, sin variar la temperatura. O dicho de otro modo, la presión parcial de un gas en una mezcla es igual a la presión total por la fracción molar del gas en cuestión.
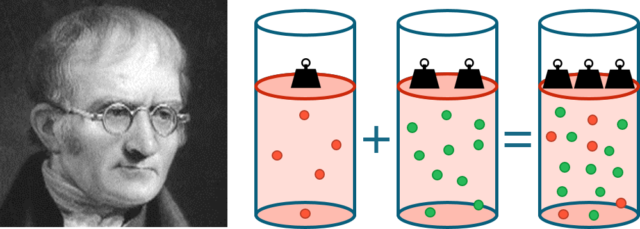
De esta forma, nuestro cuerpo está acostumbrado a respirar 0.78 atmósferas de nitrógeno y 0.21 de oxígeno, pero a profundidades mayores estas presiones también aumentan (a los 20 m que venimos usando de ejemplo las presiones parciales de nitrógeno y oxígeno se triplican), y el nitrógeno y el oxígeno a presión darán lugar a distintos efectos en nuestro cuerpo. Vamos a ver por separado estos efectos, empezando por el oxígeno.
Efectos del oxígeno a presión
El oxígeno es extraordinariamente oxidante (¡vaya polipote!): el potencial redox del oxígeno molecular (O, la forma en la que se encuentra en la atmósfera) es 1.23 voltios, solo algo menor que la del cloro molecular, 1.36 V. Tras la Gran Oxidación, a los organismos terrestres no nos ha quedado otra que adaptarnos a esta atmósfera tan oxidante, pero a una presión tisular de oxígeno de sólo media atmósfera (equivalente a respirar aire a 14 m de profundidad) ya se produce hiperoxia, el oxígeno empieza a tomar un carácter tóxico. La toxicidad del oxígeno depende tanto de su presión como del tiempo que lo estemos respirando, con lo que esa presión parcial de media atmósfera es segura salvo si las experimentamos durante días, cosa que se puede producir en el buceo a saturación, en tratamientos de bebés prematuros o en cámara hiperbárica.
Recordemos aquí la ley de solubilidad de los gases o ley de Henry, por la que la cantidad de gas que puede disolverse en un líquido es directamente proporcional a la presión que el gas ejerce sobre su superficie.

Efecto Lorrain Smith
Cuando la presión parcial de oxígeno alcanza una atmósfera (a 38 metros de profundidad o respirando oxígeno puro en superficie) durante un tiempo superior a 12 horas se produce el modo crónico de la toxicidad del oxígeno, también llamado cuadro pulmonar o efecto Lorrain Smith por el patólogo James Lorrain Smith que lo describió en 1899, caracterizado por congestión de las vías aéreas, edema pulmonar y disminución de la difusión de los gases respiratorios y por tanto de la capacidad vital, así como daños oculares [Lorrain Smith 1899].
Afortunadamente estos daños son de carácter progresivo y reversible al cesar la exposición, en particular debido a que el exceso de oxígeno no pasa de la sangre a los tejidos por el sistema tampón (amortiguador) hemoglobina-oxígeno o efecto Bohr. Este efecto fue descrito por Christian Bohr (padre de Niels Bohr, el Nobel de física por sus trabajos sobre la estructura atómica) y establece que a un pH ácido la hemoglobina se une al oxígeno con menos afinidad. Así, cuando aumenta la tasa metabólica de los tejidos, su producción de dióxido de carbono aumenta, que a su vez da lugar a bicarbonato, ácido, lo que favorece la liberación del oxígeno transportado por la hemoglobina en los tejidos que más lo necesitan.

Efecto Paul Bert
A partir de 1.4 atmósferas o 56 metros de profundidad se produce otro mecanismo de toxicidad del oxígeno distinto, el denominado modo agudo, cuadro neurológico o efecto Paul Bert que lo describió en 1875. Se produce en tiempos cortos y su manifestación más frecuente es una convulsión de características similares a las del gran mal epiléptico que puede producir la muerte en unos 45 minutos, pero claro, si estás buceando lo más probable es que no dures tanto porque tener convulsiones bajo el agua no es muy recomendable.
Más aún, aparecen especies químicas muy reactivas como el anión superóxido , el peróxido
o los radicales hidróxilo ·OH. Nuestro cuerpo mantiene complejos sistemas de antioxidantes para deshacerse de estas especies, tales como el glutatión, vitamina C, vitamina E, y enzimas como la catalasa, superóxido dismutasa y varias peroxidasas, pero a estas presiones se acumulan en lo que se llama estrés oxidativo: los ácidos grasos poliinsaturados de las membranas celulares se oxidan y falla el mecanismo de membrana, lo que afecta especialmente a las neuronas y su delicado equilibro de electrolitos, con lo que el impulso nervioso colapsa y tenemos el efecto neurotóxico.
Efectos del nitrógeno a presión
El oxígeno que inhalamos al respirar se asocia a la hemoglobina, el torrente sangíneo lo transporta a las células y luego pasa a las mitocondrias, donde se produce la respiración celular, se genera CO que hace el camino contrario y finalmente se exhala.
¿Y qué pasa con el nitrógeno? ¿Acaso nuestros pulmones tienen filtros mágicos que lo dejan fuera? Pues no: el N (el nitrógeno en el aire también está en forma de moléculas diatómicas, como el oxígeno) pasa también a la sangre y recorre nuestro cuerpo, atraviesa la membrana de nuestras células (el nitrógeno es liposoluble), satura su interior según la ley de Henry y se exhala de nuevo. Y no pasa nada, porque el nitrógeno es inerte… a no ser que aumente su presión parcial, entonces el nitrógeno ¡también se vuelve tóxico!
Narcosis del nitrógeno
La toxicidad del nitrógeno se manifiesta como efectos narcóticos progresivos con su presión pero no depende del tiempo durante el cual se respire; el deterioro es completamente reversible al disminuir la exposición.
El mecanismo es una interferencia en los procesos electroquímicos necesarios para el intercambio de potencial eléctrico en los botones sinápticos, debido a la variación introducida por el N en el potencial de membrana y la consiguiente alteración del potencial de iones sodio (
), cloro (
) y potasio (
) a ambos lados. Este mecanismo de acción explica muy bien el hecho de que al disminuir la presión se restablezca el correcto intercambio iónico en las sinapsis, por lo que el efecto anestésico desaparece de inmediato [Narcosis nitrógeno].
Los primeros efectos son una disminución del pensamiento abstracto complejo (esta pérdida se sufre a muy baja cota) y la incapacidad para la multiatención. Cuándo y cómo aparecen depende muchísimo de cada persona. Estadísticamente se ha comprobado que están más predispuestas a sufrir narcosis del nitrógeno las personas gruesas, de temperamento nervioso y estresadas. Otros factores potenciadores son el ejercicio físico (conviene evitarlo antes, durante y tras la inmersión), pasar frío, la deshidratación (es recomendable beber antes y después del buceo) y la ingesta de alcohol.
El alcohol reduce la efectividad con la que el cuerpo humano elimina el nitrógeno acumulado en los tejidos al reducir el flujo sanguíneo. Medio en broma se habla de la regla del Martini: por cada 15 metros de profundidad, el nitrógeno tiene el efecto intoxicante de un Martini con el estómago vacío. Ya que la intoxicación por alcohol y por nitrógeno suman sus efectos, beber dos copas antes de una inmersión a 15 metros, produce el mismo efecto intoxicante que una inmersión a 45 metros sin haber bebido [Buceo y bebida].

Sea como sea nadie se libra de ciertos efectos narcóticos a unos 30 ó 35 m de profundidad. A esta cota se puede experimentar un aumento de la confianza en uno mismo, pérdida de la capacidad para el razonamiento fino y euforia moderada [Inoriza 2012]. Como dice el precioso documental sobre espeleobuceo Túnel de la Atlántida: Viaje a lo desconocido del programa Al filo de lo imposible, «La gran paradoja es que aquí, lo peligroso es estar contento», y también «Si dos por dos siguen siendo cuatro, y esto no provoca hilaridad, es que todo va bien» [Narcosis].
Borrachera de las profundidades
A partir de unos 40 metros, los efectos narcóticos pueden ser tan acusados como para poner en peligro la vida del buceador, y es cuando pasamos a llamarlo borrachera de las profundidades, término acuñado por Jacques-Yves Cousteau. Estamos hablando de desequilibrio del ánimo (con euforia o histeria extremas dependiendo de cómo haya ido la inmersion hasta ese momento), visión túnel, pensamiento irracional y despreocupación de la propia seguridad [Narcosis nitrógeno]. En el mundillo del buceo se cuenta la historia de un buceador que se quitó el regulador de la boca para ponérselo a un pez que según él se estaba ahogando…
A pesar de que todos los síntomas desaparecen al disminuir la presión y queda una amnesia parcial de lo ocurrido, el buceador no lo hará por si solo porque ha perdido la capacidad de autoanálisis, lo que le conducirá irremisiblemente al ahogamiento si no recibe ayuda para el ascenso. Por eso es fundamental no bucear jamás sin compañía, lo que se conoce como buddy diving.
Enfermedad descompresiva
Y bueno, si todo el problema fuese bucear un poco borrachuzo… pero hay más. Por la ley de Henry el nitrógeno (y cualquier otro gas inerte) a presión se perfunde poco a poco en nuestros tejidos hasta que la presión parcial de los tejidos se iguala a la de la sangre, como en el buceo de saturación. El caso es que querremos volver a la superficie en algún momento y las presiones querrán volver a igualarse, con lo que el nitrógeno abandonará los tejidos pasando de nuevo a la sangre.
Pero ¿qué pasa si lo hace muy deprisa debido a que el gradiente de presión y potencial químico sea alto? Pues que lo hará a ebullición, produciendo burbujas en los vasos sanguíneos y en las articulaciones, que pueden dar lugar a bloqueo circulatorio (isquemia). Desde luego nada bueno. Es lo que se llama síndrome de descompresión o enfermedad descompresiva (DCS, decompression sicknes) [Enfermedad descompresiva 1].
La enfermedad descompresiva se identificó en 1841 en los mineros de la primera mina de carbón presurizada del mundo, pero se generalizó en obreros trabajando en seco pero por debajo del nivel del agua, en una especie de gran caja sumergida y con aire bombeado desde superficie, y por tanto en condiciones hiperbáricas, que se utilizaba por ejemplo en la cimentación de puentes en ríos. A los pozos de cimentación se les solía llamar por el término francés caisson, con lo que una mala traducción hizo que a la enfermedad descompresiva se le llamase en España «enfermedad de los cajones» [Enfermedad cajones]. A los pocos minutos de la salida algunos trabajadores presentaban manchas en la piel, dolores articulares punzantes, y en ocasiones lesiones neurológicas más serias [Enfermedad descompresiva 2].
Los trabajadores del puente de Brooklyn en torno a 1880 compararon la postura al retorcerse por el dolor provocado por la enfermedad descompresiva con la moda femenina de la época de adoptar lo que se llamaba la «curva griega«, derivada a su vez de la curva praxitelilana, así que incluso hoy en día a la enfermedad descompresiva en inglés se la conoce como «the bends.» Paul Bert explicó las causas en 1878.

Pero como medir la velocidad de ascenso no es práctico se utiliza la idea de hacerlo escalonadamente con lo que se llaman paradas de descompresión. Las primeras tablas de descompresión las construyó John Scott Haldane en 1908 experimentando con cabras y cobayas (eran otros tiempos), lo que redujo drásticamente la incidencia de la enfermedad descompresiva en los buceadores. Haldane usó un modelo con un pequeño número de compartimentos (cinco) que simulan los tejidos («tejidos hipotéticos»), idea que, con algunas mejoras, utilizan todas las tablas y ordenadores de buceo de la actualidad (ver abajo) [Haldane 1908].
El siguiente avance lo hizo la US Navy en 1937 mediante prueba y error usando el método de la bisección: mandamos 10 aguerridos soldados a 18 m durante 70 minutos y al subir 5 casi pasan a mejor vida (había que tratarlos en una cámara hiperbárica donde se les descomprimía con cuidado), luego otros 10 buceadores durante 50 minutos y todos suben felices, seguido de otros 10 durante 60 minutos lo que resulta en que solo dos están mal (se permitían una tolerancia de dos buceadores enfermos)… Eso produjo perfiles de inmersión «seguros» (si tienes la edad, sexo, físico y entrenamiento de un buceador de la armada y no te importa sufrir la enfermedad descompresiva un 20% de las veces) [Medicina buceo].
Luego llegó la NAUI (National Association of Underwater Instructors) y viendo que el buceo recreativo se estaba popularizando y aumentaban los accidentes, cogió las tablas de la US Navy y las modificó haciéndolas más conservadoras: el ratio de profundidad/tiempo de 18 m/60 minutos pasó a 18m/55 minutos. Con algunas modificaciones esas son las tablas que se usan hoy en día: utilizando como profundidad la máxima alcanzada (que debe ser al principio de la inmersión) y el tiempo de inmersión, las tablas indican el número de las paradas que hay que hacer, a qué profundidad y durante cuánto tiempo.
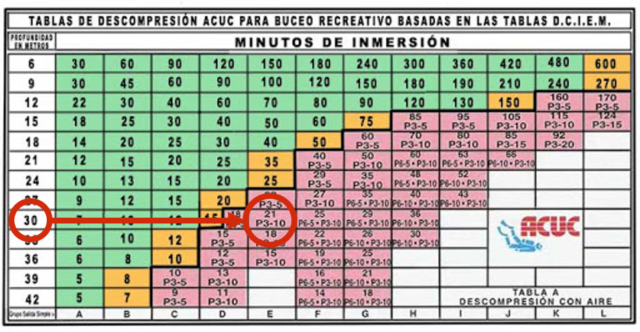
En realidad estas tablas ya no se usan porque tenemos ordenadores de buceo que integran el perfil de la inmersión en vez de usar la profundidad máxima, lo que redunda en inmersiones más largas con total seguridad. Además tienen en cuenta otros factores como la temperatura del agua, el tiempo entre inmersiones sucesivas y muestran el tiempo de no fly (el periodo tras una inmersión en la que no se debe volar debido a que la presión de cabina es inferior a la atmosférica y se podría producir la enfermedad descompresiva; los vuelos de accidentados en buceo hay que hacerlos a baja rasante, por debajo de 300 m). Los ordenadores son una herramienta indispensable para el buceo moderno.

Otras consideraciones
Profundidades límites de seguridad
Los riesgos de hiperoxia y narcosis dictan los límites de seguridad del buceo autónomo con aire. El primer nivel de certificación de buceo según la entidad certificadora [PADI] (otras entidades certificadoras usan otros nombres) se llama Open water y permite descender hasta los 18 m de profundidad, que se amplían hasta los 30 m con una licencia Advanced open water, profundidad a la que pueden empezar a aparecer síntomas de narcosis del nitrógeno en adultos.
Pocos buceadores optan a la certificación Deep diver que les habilita hasta los 40 m, donde hay que empezar a tener precauciones con el efecto Lorrain Smith y la borrachera de las profundidades, y sólo en casos excepcionales se permite llegar hasta los 55 m, en el borde del efecto Paul Bert. La máxima profundidad para la que existe certificación oficial respirando aire es la de nivel 3 francesa que habilita hasta los 60 m. El curso PADI Trimix Diver permite descender hasta los 90 m respirando trimix (ver abajo).

Otros gases
Algunos de los problemas derivados de respirar oxígeno y nitrógeno a presión se pueden mitigar añadiendo otros gases inertes a las botellas tales como helio o hidrógeno. La masa molecular del gas (Ley de Graham: las velocidades de difusión y efusión de los gases son inversamente proporcionales a las raíces cuadradas de sus respectivas masas molares), así como sus coeficientes de disolución en agua y en lípidos (Leyes de Fick), son determinantes para su potencia narcótica. Así, el helio tiene una potencia narcótica muy baja, pero es carísimo, difícil de conseguir y puede dar lugar a otros problemas. El hidrógeno tiene también sus ventajas pero es explosivo. Otros inconvenientes de ambos son, por una parte, que al expandirse te dejan literalmente helado, con lo que hay que protegerse del frio extra, y por otra que al ser gases inertes el problema de la enfermedad descompresiva persiste.
Hay toda una suerte de mezclas de gases a disposición de los buceadores expertos, cada una con sus ventajas e inconvenientes. Por ejemplo las dos últimas de la figura siguiente se llaman mezclas de profundidad porque tienen tan poco oxígeno que no se pueden respirar cerca de la superficie, así que se desciende con otra mezcla y se cambia a estas cuando la presión parcial de oxígeno es suficiente.
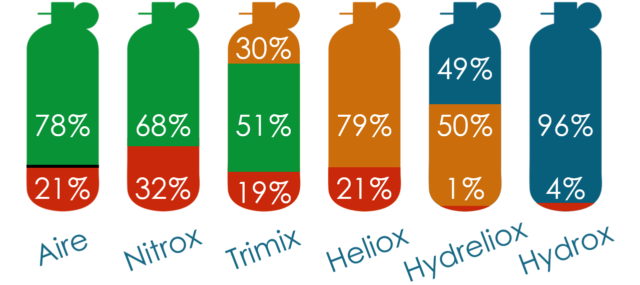
El record de profundidad alcanzada con equipo autónomo lo consiguió el egipcio Ahmed Gabr en 2014 cuando descendió hasta los 332 m de profundidad. Bajó en apenas 15 minutos, pero tardó casi 15 horas en subir, haciendo múltiples paradas programadas usando 60 botellas con distintas mezclas de gases ancladas a lo largo de un cable [Ahmed Gabr].

Buceo en altura
El buceo en altura (como en lagos, ibones…) tiene la circunstancia de la menor presión atmosférica. En general no hay que tomar precauciones especiales por debajo de unos 100 m de altitud, y hasta 300 m sólo si la inmersión va a ser profunda (más allá de 40 m). A mayor altura es preciso tenerlo en cuenta, para lo cual existen tablas de descompresión específicas o configuraciones del ordenador de buceo a tal efecto.
Afecta significativamente el tiempo que el buceador haya permanecido en altura (por ejemplo el periodo de aclimatación) porque durante ese tiempo habrá liberado nitrógeno. De forma semejante, hay que tener cuidado si tras la inmersión se va a seguir ascendiendo (no hay problema si se desciende).
En 1968, Jacques-Yves Cousteau y su equipo exploraron las profundidades del lago Titicaca en busca del antiguo tesoro inca a una altitud de casi 4000 metros. Pero el record de la inmersión a mayor altitud lo ostenta el polaco Marcel Korkus en un reservorio natural de agua a 6395 m en el volcán Ojos del Salado, en Argentina, el 13 de diciembre de 2019. Korkus y su equipo tuvieron que lidiar con una capa de hielo de 1.3 m y una temperatura del agua de 3ºC; la inmersión no llegó a los 2 m de profundidad [Altitud].
Conclusión
Quería concluir esta serie de entradas sobre la ciencia del buceo diciendo que bucear no es una actividad especialmente peligrosa, pero no está exenta de cierto riesgo. Al año mueren en el mundo 200 personas buceando, lo que supone una peligrosidad por unidad de tiempo aproximadamente 50 veces mayor que conducir un coche, o una muerte por cada doscientas mil inmersiones [Riesgo].
Afortunadamente la práctica totalidad del riesgo al bucear depende de nosotros mismos, y se puede mitigar de forma muy eficaz respetando unas normas muy sencillas:
- Mantén el equipo de forma adecuada y revísalo antes de cada inmersión.
- Respira todo el rato: no contengas la respiración.
- No pongas nada entre ti y la superficie: no te metas ni en cuevas ni en pecios.
- No bucees solo, hazlo siempre con al menos un compañero y tenlo localizado en todo momento: os cuidáis mutuamente.
- Haz caso al ordenador de buceo: asciende despacio y haz las paradas de descompresión que el ordenador indique.

Dedicatoria
Esta serie de entradas sobre la ciencia del buceo están dedicadas in memoriam a José Cervera, @Retiario, una de las personas más extraordinarias que he tenido la suerte de conocer y con quien compartía tres pasiones: la ciencia, la esgrima y el buceo.

Nos vemos en el Gran Azul, Maestro.
Bibliografía
- [Ecuación hidrostática] Mecánica de fluidos I: Principio fundamental de la hidrostática – El Tamiz – https://eltamiz.com/2013/01/10/mecanica-de-fluidos-i-principio-fundamental-de-la-hidrostatica/ (consultada el 28-mar-2021)
- [Tonel Pascal] Tonel de Pascal: cómo funciona y experimentos – Fanny Zapata en lifeder.com – https://www.lifeder.com/tonel-de-pascal/ (consultada el 02-ene-2021)
- [Diccionario buceo] Diccionario de buceo – ExtraSub, buceo seguro – https://www.extrasub.com/diccionario-buceo (consultada el 02-ene-2021)
- [Cronograma leyes gases] Cronograma leyes de gases – Sutori: Transform your lessons into collaborative learning experiences – https://www.sutori.com/item/edme-mariotte-1620-1684-fue-un-abad-fisico-y-quimico-frances-estudio-la-compr (consultada el 02-ene-2021)
- [Valsalva] Antonio Maria Valsalva – EcuRed, enciclopedia cubana – https://www.ecured.cu/Antonio_Maria_Valsalva (consultada el 02-ene-2021)
- [AquaViews] 10 Tips to Equalize Your Ears When Scuba Diving – AquaViews: SCUBA Magazine – https://www.leisurepro.com/blog/scuba-guides/10-tips-to-equalize-your-ears-when-scuba-diving/ (consultada el 02-ene-2021)
- [Ranna 2016] Prevalence of dental problems in recreational SCUBA divers: a pilot survey. V. Ranna, H. Malmstrom, M. Yunker, C. Feng y S. Gajendra. British Dental Journal, 221(9):577-581 (2016) – https://doi.org/10.1038/sj.bdj.2016.825
- [Lorrain Smith 1899] The pathological effects due to increase of oxygen tension in the air breathed. J. Lorrain Smith. J Physiol, 24, 19-35 (1899) – https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1516623/
- [Narcosis nitrógeno] Narcosis nitrogenada o Borrachera de las profundidades – ACUC blog – http://acuc.es/blog/narcosis-nitrogenada-o-borrachera-de-las-profundidades/ (consultada el 04-ene-2021)
- [Buceo y bebida] El buceo y la bebida – M@are Nostrum – http://marenostrum.org/buceo/medicina/bebida/index.htm (consultada el 02-ene-2021)
- [Inoriza 2012] Fisiología en situaciones especiales: buceo, grandes alturas y vuelos aeronáuticos y espaciales. J.M. Inoriza, N. Estanyol, M. Robert, R. Galán y A. Villalonga. Capítulo del libro Fisiología aplicada a la Anestesiología, 417-427 (2012) –https://www.researchgate.net/publication/299637021_Fisiologia_en_situaciones_especialesbuceo_grandes_alturas_y_vuelos_aeronauticos_y_espaciales
- [Narcosis] Túnel de la Atlántida: Viaje a lo desconocido – Al filo de lo imposible – https://www.rtve.es/alacarta/videos/al-filo-de-lo-imposible/filo-imposible-tunel-atlantida-viaje-desconocido/5016587/ (consultada el 31-dic-2020)
- [Enfermedad descompresiva 1] Diving Science: Everything You Never Wanted to Know about Decompression Sickness – Helena Bell en Medium – https://medium.com/@HelBell/diving-science-everything-you-never-wanted-to-know-about-decompression-sickness-7214cb1e684 (consultada el 04-ene-2021)
- [Enfermedad cajones] Enfermedad de Caisson – Epónimos de la Faculta de Medicina de la UFM – https://medicina.ufm.edu/eponimo/enfermedad-de-caisson/ (consultada el 02-ene-2021)
- [Enfermedad descompresiva 2] DCS History – Gamma divers – https://gammadivers.com/dcs-history/ (consultada el 31-dic-2020)
- Haldane 1908] The Prevention of Compressed-air Illness. A.E. Boycott, G. Damant y J.S. Haldane. The Journal of hygiene, 8 3, 342-443 (1908) – https://doi.org/10.1017%2FS0022172400003399
- [Medicina buceo] The Physician’s Guide to Diving Medicine. C.B. Carlston, R.A. Mathias y C.W. Shilling (editores). Springer Science & Business Media. ISBN: 0306414287 (1984) – https://books.google.es/books?id=OSzjBwAAQBAJ&dq=The+Physician%E2%80%99s+Guide+to+Diving+Medicine&hl=es&source=gbs_navlinks_s (consultada el 03-ene-2021).
- [Tabla ACUC] La descompresión en buceo. Aproximación al cálculo – ACUC blog – http://acuc.es/blog/la-descompresion-en-buceo-aproximacion-al-calculo/ (consultada el 31-dic-2020).
- [Dive Inn]. Web de la empresa Dive Inn – https://www.scubastore.com/buceo-submarinismo (consultada el 03-ene-2021)
- [PADI] Professional Association of Diving Instructors – https://www.padi.com/es (consultada el 01-ene-2021)
- [Ahmed Gabr] Sitio oficial de Ahmed Gabr – http://www.ahmedgabr.com/ (consultada el 01-ene-2021)
- [Altitud] Highest altitude scuba dive – Guinness World Records – https://www.guinnessworldrecords.com/world-records/scuba-diving-highest-altitude (consultada el 01-ene-2021)
- [Riesgo] Scuba Diving: What Are the Risks? – GenRe perspective blog – https://www.genre.com/knowledge/publications/uwfocus15-2-beijer-en.html (consultada el 01-ene-2021)

Me licencié y doctoré en química con una Tesis sobre la simulación por ordenador del ADN, pero cuando hacía la maleta para el post-doc se me presentó la posibilidad de trabajar haciendo cositas para misiones espaciales, y en eso ando. Comunico ciencia desde el Twitter Apuntes de ciencia. Más acerca de mi (incluyendo mis artículos y presentaciones online) aquí.
