Primera temporada, tercer capítulo. Estamos conociendo al profesor de química Walter White y a su alter ego todavía naciente… Ya han empezado los dilemas morales con la muerte de Emilio y con Loco8 encadenado en el sótano de Jesse Pinkman. Es entonces cuando Loco8 llama a White por su nombre y deja claro que Jesse…
Primera temporada, tercer capítulo. Estamos conociendo al profesor de química Walter White y a su alter ego todavía naciente… Ya han empezado los dilemas morales con la muerte de Emilio y con Loco8 encadenado en el sótano de Jesse Pinkman. Es entonces cuando Loco8 llama a White por su nombre y deja claro que Jesse le ha contado todos los detalles de la vida personal del profesor incluyendo detalles de su forma de dar clase. Y es que lo que Pinkman recuerda de esas clases es que hicieron un refresco de uva para aprender qué era el dióxido de carbono o CO2.
Loco8 vía
¿Cómo pudo hacerse este experimento del refresco de uva? Con esta pregunta en la cabeza Javi Fernández Panadero y yo empezamos a devanarnos los sesos. Y salieron cosas muy interesantes que acabaron plasmándose, como no podía ser de otra manera con semejante maestro, en la realización de un experimento.
Hablamos de fruta carbonatada como en este vídeo, de usar bicarbonato sódico para producir CO2 como aquí, y de producir hielo seco de manera casera como en este otro vídeo. Y haciendo un batiburrillo con todo lo aprendido en Internet, diseñamos el experimento que llevé a cabo con la inestimable ayuda de mi hermana Carmen.
Para ello, compramos zumo de uva (lo encontramos en El Corte Inglés), y en Amazon conseguimos cartuchos de CO2 Massi 38655 para bicicleta junto con el regulador Massi 43995 de CO2. ¡Todo listo! La idea era probar distintos métodos y determinar cuál era el mejor para hacer refresco de uva a lo “Breaking Bad”.
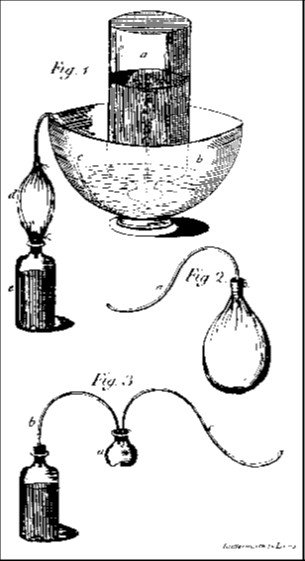
El primer método era el más sencillo: el zumo de uva contiene varios ácidos, entre ellos el cítrico, que en contacto con bicarbonato sódico produce burbujas de CO2. Como curiosidad histórica, el químico Joseph Priestley publicó un artículo en 1772, en el que produce el CO2 a partir de tiza (carbonato de calcio) y ácido sulfúrico, introduciéndolo por medio de un tubo flexible en un recipiente con agua. Parece ser que la inspiración le vino en una cervecería: en la fermentación (ya sea de la cebada o de la uva) se producen alcohol y CO2.
Montaje de Joseph Priestley
La segunda forma que queríamos probar consistía en añadir el CO2 directamente. Contábamos con que al salir el gas CO2 del cartucho este se enfriaría de manera que aumentaría la solubilidad del gas en la disolución acuosa del zumo de uva. El tercer método era usar el cartucho y un trapo para producir hielo seco: el CO2 en estado sólido se sublima pasando directamente a estado gaseoso (sin pasar por el estado líquido) de manera que obtenemos el CO2, y al estar tan frío (alcanza temperaturas de -78ºC) aumentamos también la solubilidad.
En botellas de refresco vacías de 33 cl, añadimos 30 ml de zumo de uva. Usamos la primera botella como control y el resto para experimentar.
En el vídeo (perdonad la calidad casera) se van explicando los distintos pasos que seguimos. Pudimos comprobar que los tres métodos incorporaban CO2 ya que la muestra se acidificaba (el CO2 en solución acuosa está en equilibrio con el ácido carbónico). En el caso del bicarbonato, una cucharada resultó ser demasiado para los 30 ml de zumo de uva. Al abrir las botellas al final del experimento la que más gas tenía era la del hielo seco, sin embargo, en la cata posterior la que más había incorporado gas era la tercera.
Ahora lo ideal sería repetir el experimento con mayor cantidad de muestra, pero para ello, hay que encargar más cartuchos de CO2. Y ya que estamos (lo siento Mr. White) cambiaría el zumo de uva por zumo de limón que tiene mayor ácido cítrico.